清华团队生物3D打印“活”神经组织,加速神经网络再生!!!清华大学材料学院王秀梅教授团队与清华长庚医院王贵怀主任团队在《BioactiveMaterials》期刊上发表了一项名为“3Dbioprinteddynamicbioactivelivingconstructenhancesmechanotransduction-assistedrapidneuralnetworkself-organizationforspinalcordinjuryrepair”的研究,成功开发出一种创新的“动态活性生物墨水”(GHP),并通过生物3D打印技术构建出功能化的类神经组织。该组织能显著增强神经干细胞的机械转导能力,加速功能化神经网络再生,最终在大鼠脊髓全断模型中有效促进神经再生及运动感觉功能恢复,为攻克脊髓损伤修复这一世界性难题提供了突破性新策略。

01
研究背景
脊髓损伤(SCI)后的神经再生修复是全球性医学难题,临床缺乏有效治疗手段。生物3D打印技术通过精准构建“仿生基质-干细胞”微模块组装体,为神经再生提供了新途径。这类“活”的组织替代物能传递信号,引导神经干细胞(NSC)自组织形成功能性神经网络。然而,神经组织高度复杂,如何优化基质材料设计以深化细胞-材料相互作用、提升构建组织的神经功能性,是当前研究的核心挑战。
02
研究方法
清华大学材料学院王秀梅教授团队与清华长庚医院王贵怀主任团队,受天然神经组织细胞外基质(ECM)动态力学特性启发,设计并制备了一种名为GHP的动态活性生物墨水。
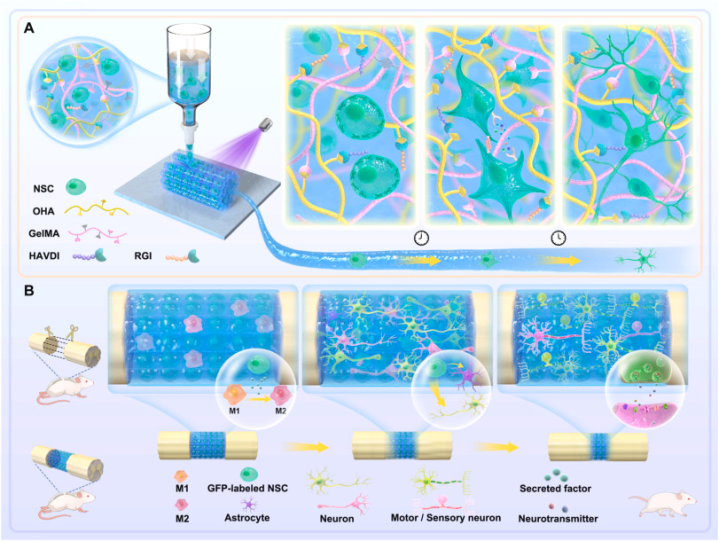
图1. 动态活性生物墨水(GHP)设计原理图
材料构建
GHP由甲基丙烯酰化明胶(GelMA)、氧化透明质酸(OHA)作为基础水凝胶网络,并引入N-钙粘蛋白模拟肽(HAVDI)和脑源性神经营养因子模拟肽(RGI),通过共价交联(光固化)和动态可逆交联(席夫碱键)形成双交联网络。
墨水特性表征
系统评估了GHP的物理化学性质,包括含水率、亲水性、渗透性、储能模量、杨氏模量、自愈合能力、应力松弛特性及营养物质扩散能力。验证了其优异的生物可打印性和维持包载NSC高活力的能力。
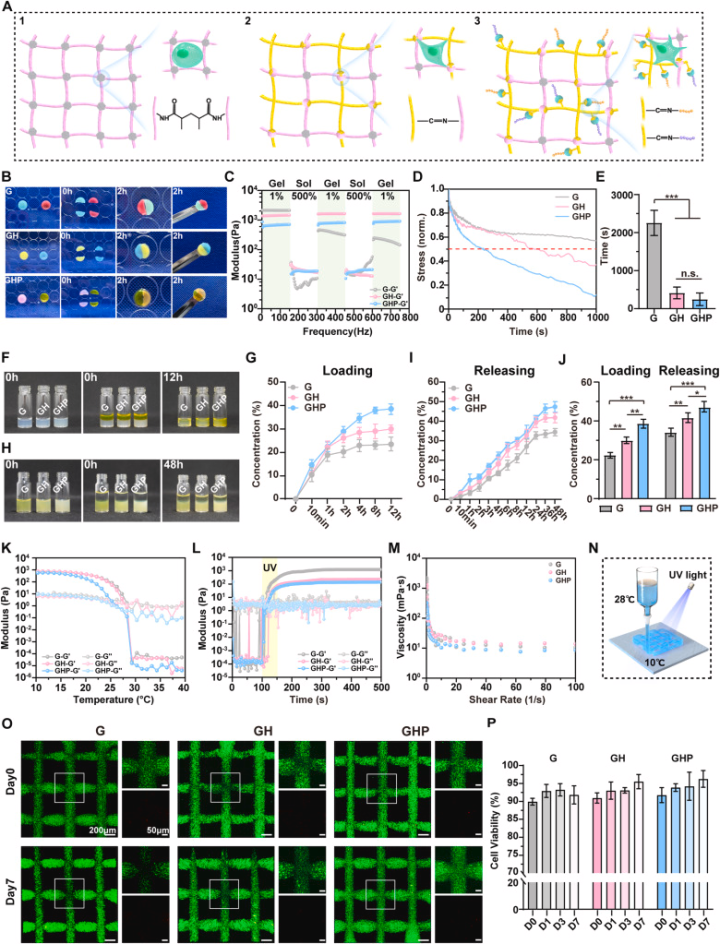
图2. GHP墨水的制备流程与物理特性
体外机制研究
在3D打印构建的类神经组织支架中,深入研究GHP墨水如何通过其结构动态性和HAVDI/RGI生物活性信号,调控NSC的粘附、迁移、形态发生、机械转导、神经营养因子分泌及神经元分化。利用RNA测序分析其分子机制。
体内功能验证
将负载NSC的生物3D打印仿生神经纤维(GHP@NSC)移植至大鼠脊髓全横断损伤模型。通过组织学、免疫荧光染色、行为学测试等方法,追踪移植后NSC的分化命运(4周、12周),评估神经网络自组织、与宿主整合情况,以及大鼠运动、感觉功能恢复效果。
03
核心发现
墨水特性优异
GHP墨水具备高含水率、良好亲水性与渗透性、较低的模量(更柔软),其动态网络赋予出色的自愈合、应力松弛和营养扩散能力,为NSC提供适应性微环境。
增强机械转导与细胞行为调控
GHP墨水的结构动态性(主要通过席夫碱键实现)显著增强了NSC的机械感应和机械转导能力(即细胞感知并响应机械力的能力)。这促进了NSC的神经突生长(形态发生)、神经营养因子分泌及向神经元的分化。
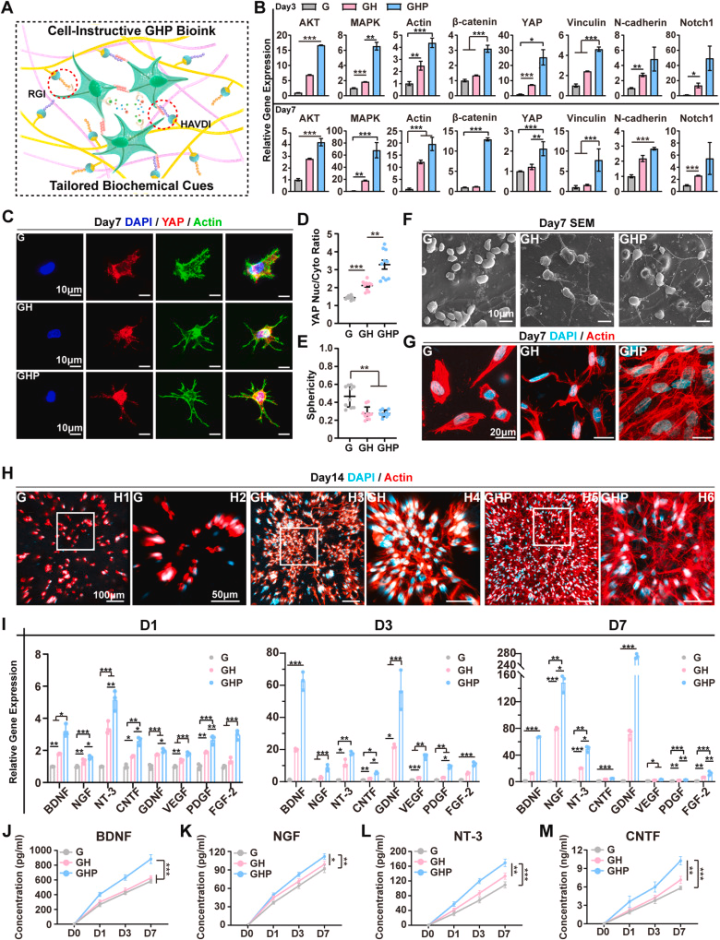
图3. GHP墨水动态性增强NSC机械转导
生物活性信号协同加速神经网络构建
RNA测序证实,引入的HAVDI肽(粘附信号)和RGI肽(神经营养信号)与墨水的动态性协同作用,精准调控细胞-基质和细胞-细胞相互作用,显著加速了生物3D打印类神经组织内部功能性神经网络的形成。
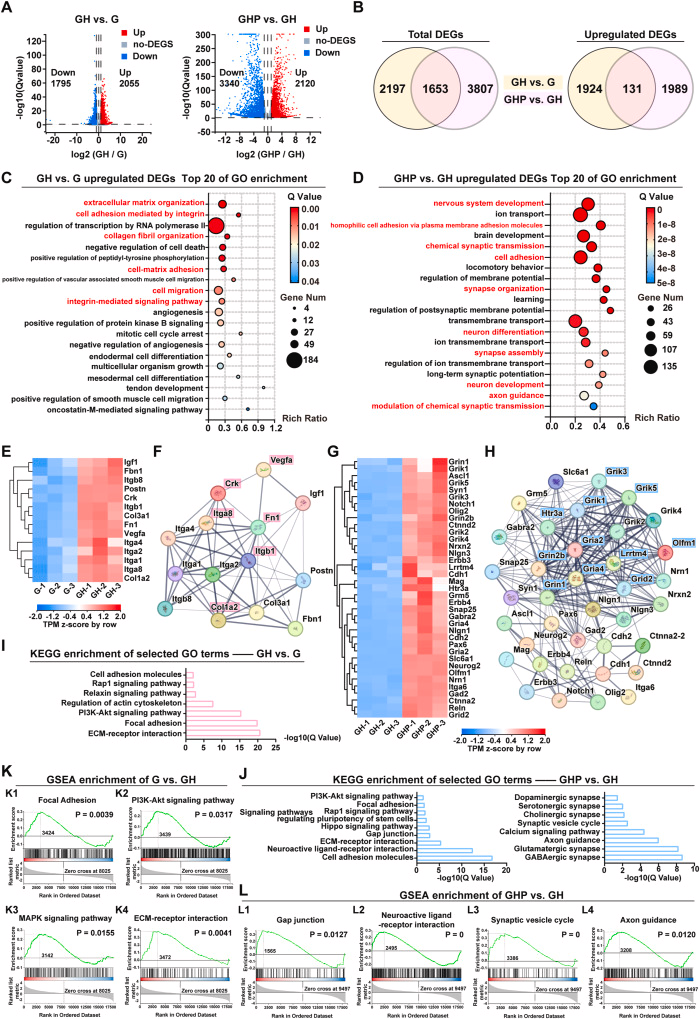
图4. RNA测序揭示GHP加速神经网络构建的分子机制
体内高效修复
高效分化:移植4周后,GHP@NSC中的NSC绝大多数分化为新生神经元,少量分化为星形胶质细胞。
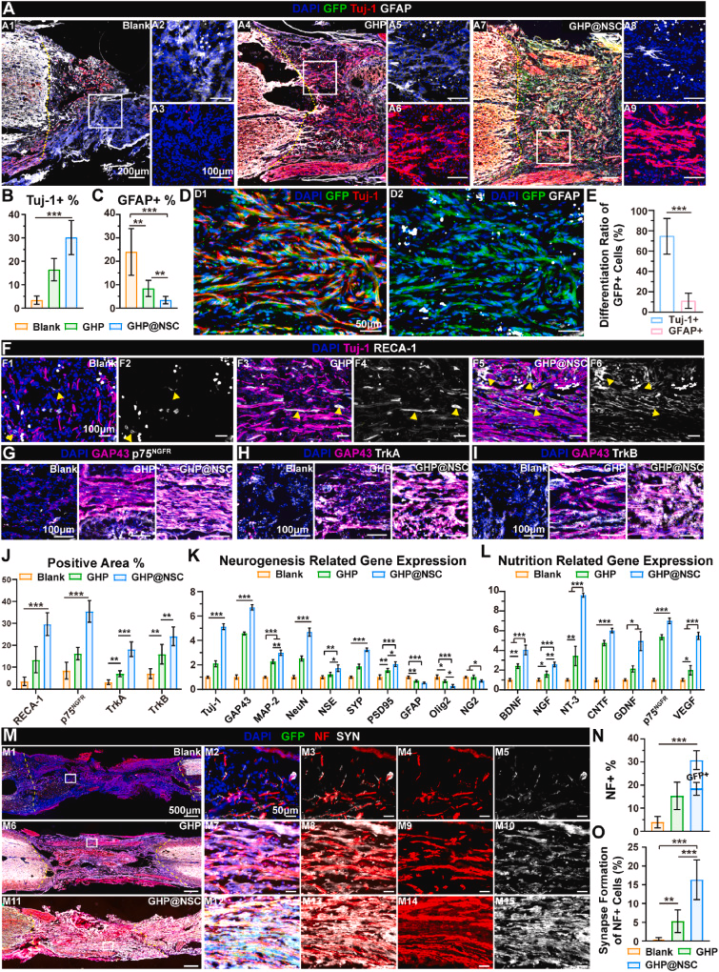
图5. GHP@NSC移植4周后高效促进神经再生
自组织与整合:移植12周后,GHP@NSC在损伤区成功自组织形成功能化神经网络,并有效整合入宿主神经网络。
功能恢复:接受GHP@NSC移植的脊髓损伤大鼠,其运动功能和感觉功能均得到显著恢复,证明了该策略的治疗效果。
04
研究意义与展望
本研究成功设计并应用了GHP动态活性生物墨水,结合生物3D打印技术,构建出具有显著增强的神经网络再生能力的功能性类神经组织替代物。
这清晰揭示了基质材料的结构动态性(力学适应性)与特定生物活性信号(HAVDI,RGI)在协同调控NSC命运中的关键作用,特别是阐明了通过增强机械转导加速功能性神经网络构建的核心分子机制,为理解细胞与微环境相互作用提供了新见解。
此外,该研究强调了动态力学信号在神经组织工程中的重要性,为未来设计更先进的功能化生物墨水(如整合更多动态键、响应性因子或电活性成分)提供了明确思路。同时,推动该技术向更大尺度、更复杂神经损伤修复(如脑损伤)的应用,以及探索其长期安全性和规模化生产,是下一步研究的重点。
什么地方可以股票开户提示:文章来自网络,不代表本站观点。


